吗替麦考酚酯是一种抗代谢类免疫抑制剂,新型免疫抑制剂,对淋巴细胞具有高度选择作用,能减少急性排斥反应的发生,且肝肾毒性作用较轻。
品种详情
吗替麦考酚酯
 我感兴趣
我感兴趣
英文名称:Mycophenolate Mofetil
分类:抗肿瘤和免疫调节剂
医保:全国19版 乙类
DMF备案: USDMF CDMF备案中
品种咨询
调研报告
关联审评资料
市场信息
供应商

产品特点


基本信息


产品发展历程


专利


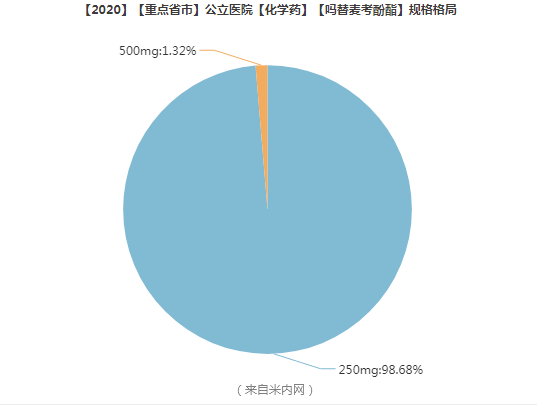
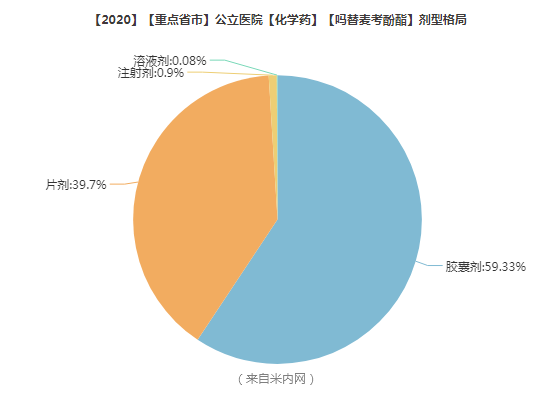
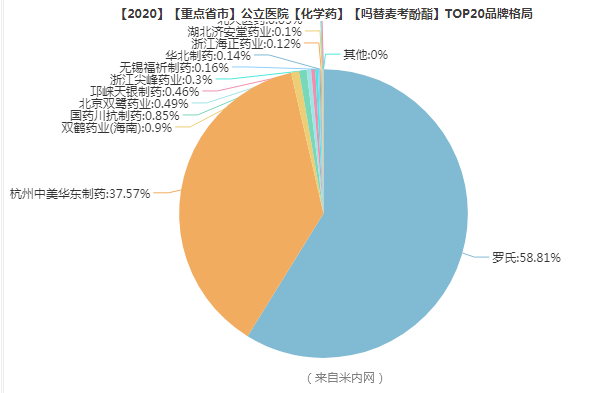
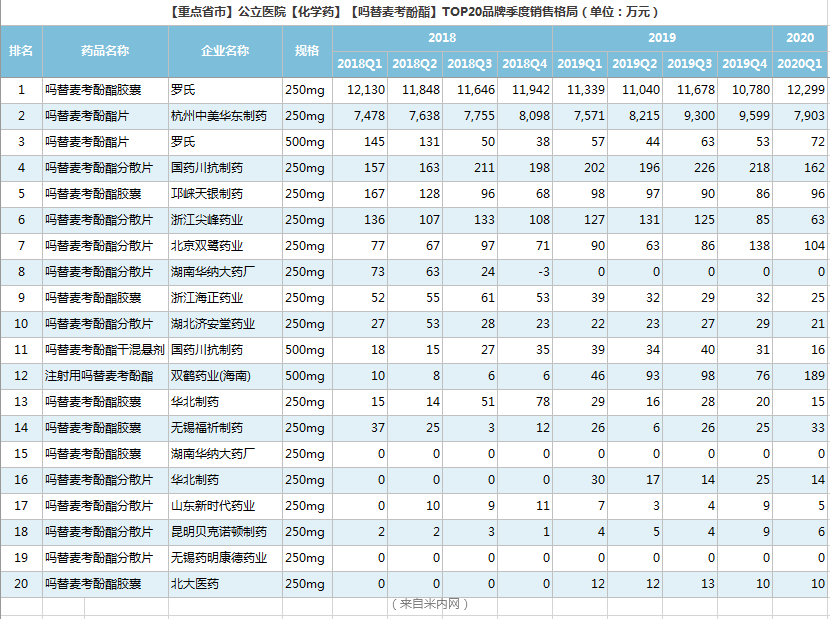
制剂市场


销售占比


注册申报


招投标价格


原料国内备案


SWOT

本品信息更新至:2020.12.28